Соляная кислота применяется в изготовлении некоторых ВВ. Сейчас является перекурсором, и приобрести ее в Химмаге не получится. Но ее достаточно просто изготовить в домашних условиях. Химически чистая концентрированная соляная кислота бесцветная, дымящаяся на воздухе жидкость (выделяется хлороводород) с резким запахом. Плотность соляной кислоты составляет 1.19, при концентрации 37 %.
Реактивы:
NaCl – поваренная соль. В принципе подойдет любой хлорид, KCl например.
H2SO4 – серная кислота. Обязательно концентрированная (обугливает спичку в холодном состоянии), вполне подойдет выпаренный электролит.
Защитное снаряжение:
Соляная кислота – ЗЛО! При попадании на кожу вызывает химические ожоги. На одежду ей тоже не следует попадать – разъедает мгновенно. Хлороводород ядовит! Получение соляной кислоты лучше производить на открытом воздухе или в хорошо проветриваемом помещении. Минимум защитных средств: 1. Резиновые перчатки (лучше как на фото). 2. Противогаз ну или респиратор (поможет вам быстро ликвидировать последствия возможной аварии без вреда для здоровья).
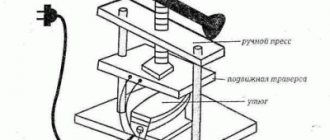
Оборудование: 1. Электрическая плитка или другой источник тепла. 2. Весы. 3. Мерный стакан. 4. Реакционный сосуд, я использовал плоскодонную колбу на 250 мл. 5. Предохранительная склянка. Прекрасно подойдет любая колба, (главное, чтобы объем склянки не был меньше объема получаемой кислоты). 6. Пара резиновых пробок. 7. Трубки, можно использовать трубки от капельниц.
В итоге должен получиться вот такой прибор.
Правда тут есть пара нюансов: 1. Трубки, используемые в приборе должны быть одного диаметра, лучше отказаться от использования иголок от шприцов в качестве штуцеров. Это создаст разность в давлении и аппарат рванет (у меня так и случилось при использовании иглы от шприца). 2. Трубку, из которой идет HCl лучше не опускать в воду, так как вода может быть засосана в систему из-за большой растворимости HCl. 3. Предохранительная склянка в принципе необязательна, можно и без нее, но если воду засосет в реакционную колбу и она может лопнуть, разбрызгивая горячую серную кислоту.
Изготовление:
1. Отвешиваем соль примерно 10-20 граммов. Кислоты возьмите примерно столько же 10-15 миллилитров. Я написал примерно потому что количество кислоты зависит от ее концентрации. Я брал 1 : 1 по объему. Если кислота 60-80%, то хлороводород сначала растворится в воде, а только потом будет выделяться.
Короче говоря, МЕНЬШЕ ВОДЫ – Меньше ПРОБЛЕМ! Так что лучше потратить побольше времени на выпаривание электролита.
2. Помещаем соль в реакционную колбу. 3. Собираем установку, проверяем все соединения, они должны быть герметичны. 4. Наливаем в мерный стакан 50-100 мл. воды (желательно дистиллированной) и вставляем в него трубку. 5. Надеваем противогаз. 6. Теперь главное быстро налить серную кислоту в реакционную колбу и заткнуть горлышко газоотводной трубкой. Противогаз спасет вас от хлороводорода, который начнет выделяться. 7. Сначала реакция идет сама, потом колбу нужно чуть-чуть нагреть. NaCl + H2SO4 → Na2SO4 + 2HCl↑
Далее приведены фотографии прибора и всего процесса:
Таким способом можно получить кислоту максимальной концентрации 37-40%. В процессе получения вы увидите, как объем воды, которую вы налили в стакан начнет увеличиваться. Продолжайте насыщать воду до тех пор, пока газ не перестанет растворятся. Хранить кислоту нужно в плотно закрытой таре, во избежании улетучивания HCl. УДАЧИ!
В настоящее время выбор аккумуляторных батарей огромен — в продаже можно найти уже готовые к использованию источники питания, а также сухозаряженные батареи, которые требуют осуществить приготовление электролита и его заливку до начала эксплуатации. Дальнейшее обслуживание аккумуляторов многие часто осуществляют в сервисах. По разным причинам может возникнуть необходимость самостоятельно приготовить раствор. Чтобы это мероприятие увенчалось успехом, следует знать, как сделать электролит в домашних условиях.
Получение кислоты в домашних условиях
Попробуем получить щёлочь или кислоту в домашних условиях с помощью подручных средств. Конечно, полученный нами препарат не будет концентрированным (это достигается с помощью специального оборудования), но характерные свойства кислоты обязательно будут заметны.
Наиболее простой способ получение кислоты в домашних условиях
будет основан на электролизе какого-либо раствора, который диссоциирует с образованием сульфат-иона. Иным способом получить кислоту тоже можно, но это связано или с получением сернистого ангидрида, или других химических препаратов, которых может не оказаться, да и все они достаточно опасны, чтобы с ними работать дома. Поэтому, получим, например, серную кислоту (разбавленную) из медного купороса. Та концентрация, которая получается из купороса — особо не опасна, к тому же, средств для её получения нужно немного. Итак, для опыта нам необходим источник тока (отлично подойдёт блок питания от 15 до 30 вольт). Анод (электрод подключаемый к плюсу) будем брать графитовый, — чтобы не растворялся. Катод – лучше взять виде графитовой пластинки, но можно также использовать медную фольгу.
Разведите раствор купороса опустите в него электроды. На катоде будем наблюдать выделение бурого рыхлого вещества – это медь.
Что такое медный купорос? Это медь, растворённая в серной кислоте. Приготовьтесь периодически вынимать катод » — » и очищать его от выделившейся на нём меди. Чем дольше продолжается опыт, тем раствор нашего электролита становится всё более светлым – из него удаляется медь. Если опустить наш индикатор в посветлевший раствор, то окраска изменится на алый цвет. Как-никак серная кислота! Конечно, она сильно разбавленная, но всё же проявляет свои свойства. Для того, чтобы более удостовериться в полученной кислоте возьмите пищевую соду и капните на неё полученной кислотой, — при этом должно наблюдаться бурное выделение газа – это углекислый газ. Серная кислота вступает в реакцию с пищевой содой, образуя при этом соль натрия (Na2SO4), воду и пузырьки углекислого газа.
Задуманное получилось! Для некоторых веществ она слабовата (т.к. сильно разбавлена) и реакции с ними Вы наблюдать не будете.
Конечно, можно увеличить концентрацию кислоты, если растворить в воде больше медного купороса или выпариванием излишка воды в полученной кислоте. Последнее проделывать не рекомендую, т.к. пары кислоты очень опасны.
- HCl — pH=1,0
- CCl3COOH — pH=1,2
- H2C2O2 — pH=1,3
- NaHSO4 — pH=1,4
- Винная кислота — pH=2,0
- Лимонная кислота — pH=2,1
- Молочная кислота — pH=2,4
- Салициловая кислота — pH=2,4
- Янтарная кислота — pH=2,7
- C6H5COOH — pH=2,8
- CH3COOH — pH=2,9
- NH4H2PO4 — pH=4,0
- H2S — pH=4,1
- NaH2PO4 — pH=4,5
- KH2PO4 — pH=4,7
- HCN — pH=5,1
- NH4Cl — pH=5,1
- H3BO3 — pH=5,3
- (NH4)2SO4 — pH=5,5
- Фенол — pH=5,5
- CaCO3 — pH=7,3
- (NH4)2HPO4 — pH=7,9
- C6H5COONa — pH=8,0
- NaHCO3 — pH=8,3
- CH3COONa — pH=8,9
- Na2HPO4 — pH=9,2
- Mg(OH)2 — pH=10,0
- KCN — pH=11,1
- NH3 — pH=11,3
- Na2CO3 — pH=11,6
- Na3PO4 — pH=12,0
- Ca(OH)2 — pH=12,4
- Na2SiO3 — pH=12,6
- K2S — pH=12,8
- NaOH — pH=13,0
Какая кислота кислее?!
Наверное, Вы когда-нибудь задавали вопрос «какая же из кислот более кислая ?!» «или какая из щелочей более едкая ?!» На этот вопрос можно ответить, рассмотрев значения pH растворов кислот и щелочей. Кислот очень много, поэтому рассмотрим лишь самые основные. Значение рН раствора зависит от концентрации. Поэтому в таблице приведены значения рН водных растворов при концентрации 0,1 моль/л. Для малорастворимых соединений, отмеченных звёздочкой, указаны рН насыщенных растворов. Чем меньше значение pH раствора, тем кислота «кислее» и наоборот, чем больше значение pH раствора, тем более едкая щелочь! Получается, что, если выпить концентрированный лимонный сок, кислотность желудочного сока… понизится !? Действительно, раствор лимонной кислоты лишь разбавит более сильную соляную кислоту, содержащуюся в желудочном соке.
Интересные факты о серной кислоте
Хотя сегодня принято изготавливать серную кислоту на специальных предприятиях, она всё же встречается в природе, причём в 100%-ом виде. Например, в Италии на острове Сицилия можно увидеть, как со дна Мёртвого моря просачивается H2SО4. Это место принято называть Озером смерти, живые существа стараются не подходить слишком близко к нему. Выделение серной кислоты со дна происходит из-за содержания в земной коре пирита.
Серная кислота может выделяться и при сильных извержениях вулкана. Такие явления достаточно опасны для людей и окружающей среды. Одними из последствий попадания H2SО4 в атмосферу могут стать климатические изменения. Серная кислота считается главной причиной, по которой выпадают кислотные дожди, а выделяется она из-за попадания в воздух диоксида серы.
Как уже было ранее замечено, серная кислота эффективно поглощает воду из воздуха. Это качество позволяет использовать её для осушения газов. Раньше было принято наливать жидкость в небольшие ёмкости и оставлять между стёклами. Это помогало предотвратить запотевание окон в комнате.
Количество исходных веществ
Чтобы приготовить электролит с заданным значением плотности, нужно взять строго определенное количество исходных веществ. В таблице ниже приведены данные по наиболее распространенным значениям плотности для разных типов электролита.
| Плотность, г/см3 | Количество воды, л | Количество кислоты, л | Количество щелочи, кг | Температура замерзания электролита, °С |
| 1,24 | 0,819 | 0,242 | -45 | |
| 1.25 | 0,809 | 0,253 | -50 | |
| 1.26 | 0,8 | 0,263 | -55 | |
| 1.27 | 0,791 | 0,274 | -60 | |
| 1.28 | 0,781 | 0,285 | -65 | |
| 1,15 – 1.21 | 3 | 1 | -19 … +35 | |
| 1.25 – 1.27 | 2 | 1 | -20 … -40 |
Для повышения допустимой температуры эксплуатации в регионах с жарким климатом или на предприятиях с высокой температурой окружающего воздуха, в щелочные аккумуляторы вводится добавка едкого лития в количестве 15-20 гр. на литр электролита.
Плотность электролита
Для заливки в аккумуляторы используются составы с точно определенной концентрацией входящих в состав веществ. Для облегчения контроля количественного состава введено понятие плотности. Это объясняется тем, что дистиллированная вода обладает плотностью, равной 1 гр/см3 и любые посторонние добавки увеличивают это значение. Серная кислота и щелочь, имеют гораздо более высокие значения удельного веса, поэтому, измеряя плотность раствора, можно легко определить состав электролита. Плотность измеряется при помощи простейшего устройства, а о том, как замерять плотность, читайте в этой статье .
Что образуется при взаимодействии
Кислотный остаток уже не так опасен, как исходный компонент. Интересно, что именно реакции с выделением углекислого газа сода обязана добавлением её в хлеб – углекислый газ, выделяющийся из-за взаимодействия с молочной кислотой, поднимает тесто и делает в нём пузырьки.
Примерно также происходит реакция нейтрализации: основание вступает в реакцию с H2SO4 и выделяется углекислый газ. Поэтому, чтобы этот химический опыт не превратился в плачевный жизненный, следует проводить его в проветриваемом помещении.
К вопросу о том, сколько соды необходимо для нейтрализации H2SO4. Если взять 1 часть кислоты, пригодится 1 часть щёлочи для реакции с ней, то есть соотношение будет 1:1. Но концентрированная кислота требует больше соды, здесь соотношение увеличится до 1:2. Раствор соды необходим 3%.
Кроме того, если необходимо оказать помощь при ожоге кислотой, то готовится раствор соды в очень приблизительном количестве: 1 чайная ложка щёлочи и на 2,5 стакана воды. Насколько эффективна реакция? В этом помогут разобраться отзывы тех, кто с ней часто сталкивается.
Рекомендовано для Вас:
Как применять и использовать кальцинированную соду в быту
Взаимодействие с металлами
Раствор соляной кислоты может вступать во многие реакции. В первую очередь с металлами, которые стоят до водорода в ряду электрохимических потенциалов. Это – последовательность, в которой элементы идут по мере увеличения такой свойственной им меры, как электрохимический потенциал (φ0). Данный показатель крайне важен в полуреакциях восстановления катиона. К тому же именно этот ряд демонстрирует активность металлов, проявляемую ими в окислительно-восстановительных реакциях.
Так вот, взаимодействие с ними происходит с выделением водорода в виде газа и с образованием соли. Вот пример реакции с натрием, мягким щелочным металлом: 2Na + 2HCl → 2NaCl +Н2↑.
С другими веществами взаимодействие протекает по похожим формулам. Так выглядит реакция с алюминием, легким металлом: 2Al + 6HCl → 2AlCl3 + 3Н2↑.
Утилизация кислоты в домашних условиях
Некоторые кислотные растворы применяются и в быту. Например, «солянка» используется для избавления от известкового налета. Ее также используют с целью удаления ржавых пятен с одежды.
Популярные статьи Варианты поздравлений с 8 Марта
Уксусная кислота входит в состав всем известного уксуса и уксусной эссенции.
Как утилизировать уксусную кислоту с истекшим сроком годности? Чтобы утилизировать ее в домашних условиях, необходимо:
Взять пластмассовый контейнер с объемом, превышающим объем утилизируемого раствора в 2 раза. Чтобы контейнер не расплавился или не загорелся, перенести пустой контейнер в ведро со льдом. Налить воду в пустую емкость Аккуратно влить кислотный раствор в воду, обращая внимание на температуру контейнера
Важно! Нельзя лить воду в концентрированную кислоту, иначе вода может мгновенно подвергнуться кипению, а кислота – разбрызгиванию.
С помощью индикаторной бумаги (приобретается в специализированном магазине) определить рН утилизируемого раствора Чем меньше pH, тем большее количество раствора, необходимого для реакции нейтрализации, будет нужно.
Сделать раствор, необходимый для нейтрализации. Наиболее часто используемые с этой целью вещества (например, гидроксид магния) можно купить в магазинах. Осуществить реакцию нейтрализации
Приготовленные на предыдущем этапе растворы реагируют с утилизируемыми кислотами с образованием в итоге солей и воды. Процесс можно считать оконченным, если индикаторная бумажка соответствует уровню рН, равному 6 – 7. Слить полученную уже безопасную смесь в канализацию (при этом желательно, чтобы кран с водой был открыт).
Реакции с оксидами
С данными веществами раствор кислоты соляной тоже прекрасно взаимодействует. Оксиды – это бинарные соединения элемента с кислородом, имеющие степень окисления, составляющую -2. Всем известными примерами являются песок, вода, ржавчина, красители, углекислый газ.
Соляная кислота взаимодействует не со всеми соединениями, а лишь с оксидами металлов. Вследствие реакции также образуется растворимая соль и вода. В качестве примера можно привести процесс, происходящий между кислотой и оксидом магния, щелочноземельного металла: MgO + 2HCl → MgCl2 + Н2О.
Изготовление реактора попытка №2
Проблему с расплавлением реактора я решил заменив пластмасс на дерево. Из куска ОСБ я вырезал кругляш просверлил в нём всё также 3 отверстия два под электроды и один под отвод газов. Дополнил конструкцию также ещё 2 болтами что бы проще было подключать и отключать как клеммы так и электроды, плюсом также было что они повышали герметичность конструкции. Также для удобства я заменил трубу на более короткую и нанёс на низ деревянной пробки силиконовый герметик. Герметик я использовал как прокладку для герметичности.
Болты для удобства подключения
Болты для удобства подключения
Болты для удобства подключения
Теперь вроде не должен плавиться как я подумал в прицепе идея себя оправдала при испытании ни чего не расплавилось однако я упустил другой момент всё таки крышка прилегала не равномерно к банке и следовательно газ выходил из щелей так как не было достаточной герметичности. На скорую руку я постарался решить проблему обычными стяжками от части это помогло но это не решение проблемы.
Использование стяжек
Пришло время конструировать новый реактор не будем сдаваться и продолжим свои исследовательские опыты.
РАСЧЕТЫ ПРИ ПРИГОТОВЛЕНИИ РАСТВОРОВ СОЛЕЙ
Пример 1. Надо приготовить 500 г 5% раствора нитЯ рата калия. 100 г такого раствора содержат 5 г KN0 3 ;1 Составляем пропорцию:
100 г раствора-5 г KN0 3
500 » 1 — х
» KN0 3
5-500 „_ х= -jQg- = 25 г.
Воды нужно взять 500-25 = 475 мл.
Пример 2.
Надо приготовить 500 г 5% раствора СаСЬ из соли СаС1 2 -6Н 2 0. Вначале производим расчет для безводной соли.
100 г раствора-5 г СаС1 2 500 » » —х
» СаС1 2 5-500 _ х= 100 = 25 г —
Мольная масса СаС1 2 = 111, мольная масса СаС1 2 — 6Н 2 0 = 219*. Следовательно, 219 г СаС1 2 -6Н 2 0 содержат 111 г СаС1 2 . Составляем пропорцию:
219 г СаС1 2 -6Н 2 0-111 г СаС1 2
х
» СаС1 2 -6Н 2 0- 26 » CaCI,
219-25 х = -jjj- = 49,3 г.
Количество воды равно 500-49,3=450,7 г, или 450,7 мл. Так как воду отмеривают мерным цилиндром, то десятые доли миллилитра в расчет не принимают. Следовательно, нужно отмерить 451 мл воды.
Свойства химического спектра
Кислота взаимодействует со многими металлами, солями. Она считается довольно сильной и стоит в одном ряду с серной. Основная реакция проявляется на все группы металлов, находящихся левее от водорода (магний, железо, цинк – электротехнические потенциалы).
Хлороводородный раствор в разбавленном виде вступает в реакцию с солями, но только с теми, которые образованы менее сильными кислотами. Известные всем натрия и кальция карбонат после взаимодействия с ним распадаются на воду и угарный газ.
Азотная кислота
– качественная реакция на солевой раствор. Для ее получения необходимо добавить в этот реактив нитрат серебра, как результат – выпадет осадок белого цвета, с которого получается азотное вещество
С помощью данной смеси воды и водорода проводят множество интересных экспериментов. Например, разбавляют его аммиаком. В итоге, получится белый дым, густой, имеющий консистенцию маленьких кристаллов. Метиламин, анилин, диоксид марганца, калий карбонат – реактивы, также поддающиеся под влияние кислоты.
Реакции с гидроксидами
Так называются неорганические соединения, в составах которых присутствует гидроксильная группа –ОН, в которой атомы водорода и кислорода соединены ковалентной связью. И, поскольку раствор соляной кислоты взаимодействует лишь с гидроксидами металлов, стоит упомянуть, что некоторые из них называются щелочами.
Так что получающаяся в итоге реакция называется нейтрализацией. Ее результатом является образование слабо диссоциирующего вещества (то есть воды) и соли.
В качестве примера можно привести реакцию небольшого объема раствора соляной кислоты и гидроксида бария, мягкого щелочноземельного ковкого металла: Ва(ОН)2 + 2HCl = BaCl2 + 2Н2О.
Другое применение кислоты в быту
Кислотным составом можно легко очистить сантехнику из фаянса от известкового налета и ржавчины, удалить мочевой камень и другие загрязнения. Для большего эффекта к средству добавляют ингибитор (например, уротропин), замедляющий химическую реакцию.
Процедуру проводят следующим образом: кислоту разбавляют водой до достижения 5 %-ной концентрации и добавляют ингибитор из расчета 0,5 г на 1 л жидкости. Полученным составом обрабатывают поверхность и оставляют на 30-40 минут (в зависимости от степени загрязнения), после чего промывают водой.
Популярные статьи Каменная шкатулочка
Слабый кислотный раствор также используется для удаления пятен от ягод, чернил или ржавчины с тканей. Для этого материал замачивают в составе на некоторое время, после чего тщательно ополаскивают и стирают в обычном режиме.
Избавление от накипи в чайнике
Для этой цели используют 3-5 %-ный раствор соляной кислоты, который наливают в чайник и нагревают до 60-80°
С в течение 1-2 часов или до тех пор, пока накипные отложения не распадутся. После этого накипь становится рыхлой и легко удаляется деревянной лопаточкой.
Эффективность метода обусловлена тем, что реагент вступает в реакцию с карбонатами магния и кальция и превращает их в растворимые соли. Выделяющийся при этом углекислый газ разрушает слой накипи и придает ему рыхлость. После удаления солевых отложений посуду тщательно моют чистой водой.
Важный момент!
Этот способ не подходит для удаления накипи в эмалированных или алюминиевых чайниках со сколами и трещинами: это приведет к коррозии металла и его сильному повреждению.
В медицине
В данной сфере рассматриваемой вещество тоже активно применяется. Разбавленная соляная кислота оказывает следующие действия:
- Переваривает в желудке белки.
- Останавливает развитие злокачественных образований.
- Помогает в лечении онкологических заболеваний.
- Нормализует кислотно-щелочной баланс.
- Служит эффектным средством при профилактике гепатита, сахарного диабета, псориаза, экземы, ревматоидного артрита, желчнокаменной болезни, розовых угрей, астмы, крапивницы и многих других недугов.
В общем, полезный препарат. Если у человека понижена кислотность желудочного сока, то ему не помешает пропить курс медикаментов, в составе которых есть соляная кислота. Неплохим вариантом является «Орто Таурин Эрго». Он увеличивает уровень соляной кислоты в желудочной среде, помогает бороться с бактериями и паразитами.
В голову пришла идея разбавить кислоту и употреблять ее внутрь в таком виде, а не в составе медикаментов? Такое практикуется, но категорически запрещено делать это без врачебной консультации и получения инструкции. Неправильно рассчитав пропорции, можно проглотить избыток раствора соляной кислоты, и просто сжечь себе желудок.
Кстати, еще можно принимать медикаменты, стимулирующие выработку данного вещества. И не только химические. Тот же аир, перечная мята и полынь способствуют этому. Отвары на их основе можно сделать самому, и пропить для профилактики.
Получение соляной кислоты в домашних условиях
Соляная кислота применяется в изготовлении некоторых ВВ. Сейчас является перекурсором, и приобрести ее в Химмаге не получится. Но ее достаточно просто изготовить в домашних условиях. Химически чистая концентрированная соляная кислота бесцветная, дымящаяся на воздухе жидкость (выделяется хлороводород) с резким запахом. Плотность соляной кислоты составляет 1.19, при концентрации 37 %.
Реактивы:
NaCl – поваренная соль. В принципе подойдет любой хлорид, KCl например.
H2SO4 – серная кислота. Обязательно концентрированная (обугливает спичку в холодном состоянии), вполне подойдет выпаренный электролит.
Защитное снаряжение:
Соляная кислота – ЗЛО! При попадании на кожу вызывает химические ожоги. На одежду ей тоже не следует попадать – разъедает мгновенно. Хлороводород ядовит! Получение соляной кислоты лучше производить на открытом воздухе или в хорошо проветриваемом помещении. Минимум защитных средств: 1. Резиновые перчатки (лучше как на фото). 2. Противогаз ну или респиратор (поможет вам быстро ликвидировать последствия возможной аварии без вреда для здоровья).
Оборудование: 1. Электрическая плитка или другой источник тепла. 2. Весы. 3. Мерный стакан. 4. Реакционный сосуд, я использовал плоскодонную колбу на 250 мл. 5. Предохранительная склянка. Прекрасно подойдет любая колба, (главное, чтобы объем склянки не был меньше объема получаемой кислоты). 6. Пара резиновых пробок. 7. Трубки, можно использовать трубки от капельниц.
В итоге должен получиться вот такой прибор.
Правда тут есть пара нюансов: 1. Трубки, используемые в приборе должны быть одного диаметра, лучше отказаться от использования иголок от шприцов в качестве штуцеров. Это создаст разность в давлении и аппарат рванет (у меня так и случилось при использовании иглы от шприца). 2. Трубку, из которой идет HCl лучше не опускать в воду, так как вода может быть засосана в систему из-за большой растворимости HCl. 3. Предохранительная склянка в принципе необязательна, можно и без нее, но если воду засосет в реакционную колбу и она может лопнуть, разбрызгивая горячую серную кислоту.
Изготовление:
1. Отвешиваем соль примерно 10-20 граммов. Кислоты возьмите примерно столько же 10-15 миллилитров. Я написал примерно потому что количество кислоты зависит от ее концентрации. Я брал 1 : 1 по объему. Если кислота 60-80%, то хлороводород сначала растворится в воде, а только потом будет выделяться.
Короче говоря, МЕНЬШЕ ВОДЫ – Меньше ПРОБЛЕМ! Так что лучше потратить побольше времени на выпаривание электролита.
Далее приведены фотографии прибора и всего процесса:
Таким способом можно получить кислоту максимальной концентрации 37-40%. В процессе получения вы увидите, как объем воды, которую вы налили в стакан начнет увеличиваться. Продолжайте насыщать воду до тех пор, пока газ не перестанет растворятся. Хранить кислоту нужно в плотно закрытой таре, во избежании улетучивания HCl. УДАЧИ!
Кислотность воды
Большинство живых организмов могут существовать лишь в средах, близких к нейтральным. Это связано с тем, что под действием ионов Н+ и ОН- многие белки, содержащие кислотные или основные группы, изменяют свою конфигурацию и заряд. А в сильнокислой и сильнощелочной средах рвётся пептидная связь, которая соединяет отдельные аминокислотные остатки в длинные белковые цепи. Из-за этого ультраосновные (сильнощелочные) растворы вызывают щелочные ожоги кожи и разрушают шёлк и шерсть, состоящие из белка. Все живые организмы вынуждены поддерживать во внутриклеточных жидкостях определённое значение кислотности среды (а так, как клетка состоит из воды на 80%, то — кислотность воды
). Природная вода способна сохранять значение рН более или менее постоянным, даже если в неё извне попадает определённое количество кислоты или основания. Если в литр дистиллированной воды внести каплю концентрированной соляной кислоты, то рН понизится с 7 до 4. А если каплю соляной кислоты добавить в литр речной воды с рН=7, показатель почти не изменится. Кислоты и основания, попадающие в природную воду, нейтрализуются растворёнными в ней углекислым газом и гидрокарбонат-ионами: Н++НСО-3→ Н2О+СО2; ОН-+СО2→ HCO-3.
Особенности технологии приготовления электролита
При самостоятельном приготовлении следует помнить следующее:
- плотность кислоты и щелочи намного выше плотности воды;
- реакции смешивания кислоты с водой и растворения щелочи происходят с выделением высокой температуры (до 80-90°С);
- кислоты и щелочи взаимодействуют с большинством металлов.
Из перечисленного следует, что посуда для приготовления электролита должна быть из материала, стойкого к действию агрессивных веществ и температуры. Наиболее соответствует этим требованиям посуда из стекла и керамики. Использование пластиковой посуды возможно при условии недопускания ее нагрева до высоких температур. Нельзя использовать эмалированную посуду, поскольку при наличии незаметных трещин в эмали будет происходить загрязнение электролита солями металлов. То же самое относится к изделиям из нержавеющей стали. Такие материалы не вступают в реакцию с водой, но производители не гарантируют ее нейтральность по отношению к агрессивным веществам.
Приготовление кислотного электролита
Высокая плотность кислоты и способность разогрева при смешивании с водой обусловили специфику приготовления раствора: кислоту нужно вливать в воду. Если поступить наоборот, то вода, оказавшись сверху, нагреется до температуры закипания и выплеснется наружу вместе с каплями кислоты.
Чтобы уменьшить нагрев, кислоту целесообразно разбавить в два этапа. На первом готовится раствор плотностью 1.40, а затем, после остывания, делают электролит необходимой концентрации. Раствор с плотностью 1.40 называют корректирующим. Он применяется для коррекции плотности электролита в рабочих аккумуляторах. После добавления кислоты в воду смесь аккуратно перемешивают стеклянной палочкой. Приготовленный электролит необходимо оставить на некоторое время (от половины до суток) для его равномерного смешивания и полного остывания.
Приготовление щелочного электролита
Необходимое количество щелочи высыпают в отмеренное количество воды и перемешивают до полного растворения. Также необходимо выдержать время, пока осадок не растворится полностью и температура не опустится до нормальной.
Раствор щелочи нужно хранить в герметично закрытой таре, не допуская попадания воздуха. Углекислый газ легко вступает в реакцию со щелочами с образованием карбонатов – солей угольной кислоты. В результате содержание активного вещества в растворе с течением времени падает.
Растворы кислоты и щелочи должны быть прозрачными или иметь легкий желтоватый оттенок. Наличие мутности отстоявшегося раствора говорит о низкой чистоте исходных компонентов и для использования в аккумуляторах непригодны.
Требования к компонентам
Нормальное протекание химических реакций предъявляет особые требования к веществам электролита. Основное требование – высокая степень чистоты материалов. Чем чище будут химические вещества для приготовления электролита, тем выше будет КПД аккумуляторов и их долговечность.
Согласно требованиям стандартов, аккумуляторная серная кислота должна содержать не менее 92 – 94% серной кислоты. Оставшиеся 6 – 8% занимает вода. Содержание солей металлов не более тысячных долей процента.
Внимание! Щелочь выпускается в сухом виде и к ней предъявляются подобные требования.
Если с перечисленными веществами вопросов обычно не возникает (ответственность за чистоту возлагается на предприятия, выпускающие материалы и торговые организации), то с водой дела обстоят несколько хуже. Многие автолюбители не делают различие между обычной и дистиллированной водой.
Вода из водопровода насыщенна растворами различных солей металлов и органических веществ. Простое кипячение в состоянии избавиться от незначительного количества солей жесткости, а остальные вещества остаются в неизменном виде. В водопроводной воде наиболее опасными для аккумуляторов являются соли железа, находящиеся там в больших концентрациях.
Активные вещества для электролита нужно разводить дистиллированной водой, которая отличается тем, что содержание солей в ней минимально. Такая вода по своим химическим и физическим параметрам практически соответствует идеальной.
Использование в пищевой промышленности
Пищевая промышленность использует Е507 при переработке различных продуктов. Основное ее применение в пищевой промышленности заключается в производстве кукурузных сиропов, особенно с высоким содержанием фруктозы. Также она часто встречается в майонезах, входит в состав лимонной кислоты, желатина, фруктозы.
Соляную кислоту можно также использовать для кислотного модифицирования кукурузного крахмала и для регулирования рН промежуточных и конечных продуктов.
Наиболее частое использование – это производство безалкогольных напитков, на которые приходится 70-75% спроса.
Е507 также используется в других областях пищевой промышленности, включая производство гидролизованного растительного белка и соевого соуса. Она используется для подкисления дробленых костей, для производства желатина и в качестве подкислителя для продуктов, таких как соусы, овощные соки и консервы.
Популярные статьи Сложный двухэтажный цветокСоляная кислота часто используется при производстве:
- искусственных подсластителей;
- лизина и хлорида холина (оба используются главным образом в качестве добавок для корма для животных);
- лимонной кислоты;
- кукурузного крахмала;
- безалкогольных напитков;
- соевого соуса.
В области строительства
Использование соляной кислоты и ее растворов – это популярный способ улучшения множества строительных процессов. Например, ее нередко добавляют в бетонную смесь, чтобы увеличить морозостойкость. К тому же так она быстрее застывает, а стойкость кладки к влаге повышается.
Еще соляную кислоту используют, как очиститель от известняка. Ее 10-процентный раствор – лучший способ борьбы с грязью и следами на красном кирпиче. Для очистки других не рекомендуется его использовать. Структура других кирпичей более чувствительна к воздействию данного вещества.
Ожоги и отравление
Каким бы эффективным ни было это средство, оно опасно. Соляная кислота, в зависимости от концентрации, может спровоцировать химические ожоги четырех степеней:
- Возникает лишь покраснение и боль.
- Появляются пузыри с прозрачной жидкостью и отек.
- Формируется некроз верхних слоев кожи. Пузыри заполняются кровью или мутным содержимым.
- Поражение достигает сухожилий и мышц.
Если вещество каким-то образом попало в глаза, надо промыть их водой, а потом содовым раствором. Но в любом случае первым делом надо вызвать скорую.
Попадание кислоты внутрь чревато острыми болями в груди и животе, отеком гортани, рвотными кровавыми массами. Как следствие — тяжелые патологии печени и почек.
А к первым признакам отравления парами относят сухой частый кашель, удушье, повреждение зубов, жжение в слизистых оболочках и боли в животе. Первая неотложная помощь — это умывание и полоскание полости рта водой, а также доступ к свежему воздуху. Настоящую помощь может оказать лишь токсиколог.
Описание
Раствор соляной кислоты относится к классу сильных. Он бесцветный, прозрачный и едкий. Хотя техническая соляная кислота имеет желтоватый цвет, обусловленный наличием примесей хлора, железа и прочих элементов. На воздухе «дымится».
Стоит отметить, что данное вещество присутствует и в организме каждого человека. В желудке, если быть точнее, в концентрации 0.5%. Интересно, что этого количества достаточно для полного разрушения бритвенного лезвия. Вещество разъест его всего за неделю.
В отличие от той же серной, кстати, масса соляной кислоты в растворе не превышает 38 %. Можно сказать, что данный показатель – «критическая» точка. Если начать увеличивать концентрацию, то вещество просто будет испаряться, вследствие чего хлороводород просто улетучится вместе с водой. Плюс ко всему, данная концентрация сохраняется лишь при 20 °C. Чем выше температура – тем быстрее протекает испарение.
Причины появления засоров
Канализационная система перемещает сточные воды с большим содержанием органики и жиров. Они налипают на стенки тонким слоем, который постепенно нарастает и превращается в полноценный засор. Как правило, он располагается неподалеку от сливного отверстия кухонных раковин или других сантехнических приборов. Чаще всего от жировых наслоений страдает сифон, изгиб которого активно собирает на себя липкие и вязкие компоненты сточных вод.
Кроме этого, частой причиной становятся посторонние предметы, попадающие в канализацию. Здесь могут оказаться волосы, бумага, строительный мусор (песок, остатки клеевых растворов), женские прокладки и другие нежелательные компоненты. Они застревают в участках изгиба или сужения труб, становятся причиной образования постоянного засора. Никакие методы, кроме механической прочистки, результатов не дают.
На чугунных трубах встречаются случаи отслоения окалины с внутренней поверхности стенок. Она остается внутри и быстро обрастает жиром, задерживает мелкие частицы органики. Решением проблемы также станет механическая чистка труб.
Зачем нужен кислотный флюс
К металлам относятся вещества большой активности. Многие из них легко и быстро окисляются в присутствии воздуха. Образующиеся оксиды под действием атмосферной влаги превращаются в гидроксиды.
Смесь продуктов окисления хорошо заметна на железных изделиях после хранения на воздухе. Называется она ржавчиной. Другие металлы также покрываются оксидным слоем, который не позволяет ничего припаять к изделию.
Справиться с проблемой помогают кислотные флюсы, самым простым их которых является паяльная кислота. Под этим названием собраны несколько разных однокомпонентных или сложных составов, многие из которых можно приготовить своими руками.
Рецепты паяльной кислоты
При проведении пайки для предварительной обработки поверхности деталей во многих случаях используют флюсы кислотного характера. Степень активности материала подбирают в зависимости от типа металла и меры его загрязнения.
В продаже есть различные средства, состав которых подобран с учетом специфики предстоящей работы. Можно сделать паяльную кислоту в домашних условиях самостоятельно.
Для этого потребуется определенные знания, элементарное умение делать химические составы и небольшая сумма денег для приобретения компонентов.
Зачем нужен кислотный флюс
К металлам относятся вещества большой активности. Многие из них легко и быстро окисляются в присутствии воздуха. Образующиеся оксиды под действием атмосферной влаги превращаются в гидроксиды.
Смесь продуктов окисления хорошо заметна на железных изделиях после хранения на воздухе. Называется она ржавчиной. Другие металлы также покрываются оксидным слоем, который не позволяет ничего припаять к изделию.
Справиться с проблемой помогают кислотные флюсы, самым простым их которых является паяльная кислота. Под этим названием собраны несколько разных однокомпонентных или сложных составов, многие из которых можно приготовить своими руками.
Что можно сделать дома
Степень кислотности флюсов отличается. К активным смесям относятся композиции с хлоридом цинка. Из школьного курса, возможно, кто-то запомнил свойства солевых растворов.
Соли в присутствии воды склонны претерпевать гидролиз. Хлорид цинка при обменных реакциях с водой образует сильную кислоту и слабую щелочь. Поэтому раствор имеет активный кислотный характер. Соляная кислота быстро удаляет оксидные вещества.
Обычно паяльную кислоту делают прибавлением 412 г цинка к 1 литру концентрированной соляной (гидрохлоридной) кислоты. Процедура это не совсем приятна и безопасна. При работе выделяются летучие кислые пары.
Работать с концентрированной солянкой следует только под вытяжкой или в респираторе, находясь в хорошо проветриваемой комнате.
С соляной кислотой
Популярностью пользуется несколько составов с хлористым цинком. Соединения цинка используются в процессе цинкования для защиты металлов от коррозии. Этот химический элемент известен устойчивостью к процессам окисления. Сделать паяльные кислоты своими руками несложно.
Для продукции из черных и цветных металлов подойдет следующее соотношение:
- хлорид цинка – минимум 25 %, максимум – 30 %;
- концентрированная соляная кислота – 0,7 %.
Оба компонента нужно быстро растворить в воде. Следует учесть, что соляная кислота – сильно летучее вещества. Работать с ней желательно под вытяжкой. Склянку с исходным реактивом нужно держать только в закрытом состоянии.
С вазелином и спиртом
Для деталей из черных и цветных металлов иногда вместо паяльной кислоты удобнее использовать пасту с кислотными свойствами.
Для ее приготовления нужно смешать насыщенный раствор хлорида цинка – 3,7 % и технический вазелин – 85 %. Для придания требуемой консистенции в смесь добавляют немного воды.
Для работы с никелем, платиной и их сплавами своими руками можно сделать паяльную смесь из хлорида цинка – 1,4 % и этилового (винного) спирта – 40 %. Оба компонента нужно тщательно растворить в воде и перемешать готовый паяльный раствор.
После пользования всеми приведенными составами паяльную зону нужно хорошо промыть обычной водой.
С канифолью
Для проведения ответственных работы с черными металлами, пайки драгоценных и цветных металлов подойдет пастообразная смесь, сделанная своими руками из канифоли – 24 % и хлорида цинка – 1 %. Все это нужно растворить в этиловом спирте. Промывать рабочую зону по окончании паяльной процедуры нужно ацетоном.
Для образования шва с повышенными прочностными характеристиками рекомендуется взять:
- канифоли – 16 %,
- хлорида цинка – 4 %,
- технического вазелина – 80 %.
Промывать место пайки после обработки такой паяльной пастой, сделанной своими руками, сложнее. Взять нужно ацетон.
Как показывает опыт, в некоторых случаях имеет смысл заменить паяльную кислоту соответствующей пастой кислотного характера.
Самодельные кислые пасты
При работе с алюминиевыми деталями часто используют флюс с олеиновой кислотой, формула которой С17Н33СООН дает представление о большой молекулярной массе. Высшая кислота имеет вязкую консистенцию, похожа на слегка тягучую жидкость.
Паяльный флюс делается следующим образом: 20 мл олеиновой кислоты, около 3 г йодида лития растворяют в стеклянной емкости на водяной бане. Однородный раствор, сделанный своими руками, после остывания переливают в стеклянный флакон для хранения.
После пайки рабочую зону промывают ацетоном, бензином или спиртом.
Для пайки нихрома можно своими руками сделать состав из 100 г вазелина, 7 г порошкообразного хлорида цинка, 7 г глицерина.
Всю массу нужно хорошо перемешать. Желательно это сделать в толстой фарфоровой чашке или специальной ступке.
Другие доступные варианты
Широко используется для обработки железных, стальных, никелевых сплавов ортофосфорная кислота. Часто ее называют просто фосфорной. Этой кислотой можно обрабатывать поверхность чистой меди.
На всех металлах фосфорная кислота не только удаляет оксиды, но и образует защитный слой.
При паяльных работах верхний слой фосфатов легко разрушается разогретым жалом паяльника. На обработанных деталях равномерно распределяется припойная масса. В результате получается прочное соединение.
Самым, пожалуй, простым вариантом замены паяльной кислоты является обычный аспирин. Раствор быстро готовится своими руками. Нужно взять обычную дешевую таблетку, растворить в небольшом количестве воды. Иногда мастера просто посыпают растолченным аспирином место пайки.
В продаже есть готовый флюс ВТС, который, по сути, также является паяльной кислотой. Аналогичное средство можно сделать своими руками.
//www.youtube.com/watch?v=Siu_1s_Hi7M
Нужно взять салициловую кислоту, вазелин, триэтаноламин. Растворить все компоненты в спирте. Флюс успешно используется для работы с медью, платиной, серебром и их сплавами.
Источник: //svaring.com/soldering/flus/recepty-pajalnoj-kisloty
Меры безопасности
Приготовление электролита представляет собой опасность из-за использования очень агрессивных веществ. Концентрированные растворы кислоты и щелочей способны вызвать труднозаживающие кислотные ожоги, а при попадании в глаза вызывают слепоту.
Перед работой следует приготовить нейтрализующий раствор для смывки случайно попавших на тело капель электролита:
- 1% раствор пищевой соды при работе с кислотой.
- Столовый уксус для обезвреживания щелочи. Уксус нужно наполовину разбавить водой.
Работать следует в резиновых перчатках и обязательно в защитных очках или маске. При попадании электролита на кожу нужно обильно промыть место попадания нейтрализующим раствором, а после промывки глаз немедленно обратиться к врачу.
Все работы производятся на открытом воздухе или хорошо вентилируемом помещении. Пары кислоты, выделяющиеся при приготовлении раствора (особенно в горячем состоянии) вызывают раздражение верхних дыхательных путей, выраженные сильным кашлем и отеком слизистых оболочек.
В качестве одежды в домашних условиях можно использовать ту, которую не сильно жалко, поскольку даже после промывки нейтрализующим раствором между волокнами ткани останется часть агрессивного вещества и вещи будут безнадежно испорчены.
Особенности транспортировки
При транзите следует соблюдать осторожность из-за резких ядовитых свойств продукта. Он взрывоопасен и относится к восьмому классу опасности, который включает ядовитые и коррозионные грузы. Допущение перевозчиком грубых ошибок при транспортировке, ставит под угрозу не только людей, но и экологию.
Перевозка происходит при соблюдении правил, гарантирующих безопасность населения. Требуется подобрать устойчивую ёмкость для транзита. Цистерны должны быть изготовлены из сплавов, которые не разрушатся под воздействием ядов. Для перевозки опасных токсинов подойдут сернокислотные химические резервуары. При необходимости поддерживать температуру, как с дымящейся жидкостью, подбираются цистерны-термосы. Для обычного груза подойдёт сернокислотная канистра.
Транспортировка допускается лишь на автомобилях со специальной маркировкой, предупреждающей об опасном грузе. Перевозить цистерны имеют право водители, получившие свидетельство АДР, подтверждающее их компетентность. Они не ограничены во времени при перевозке, поскольку обязаны соблюдать скоростной режим для исключения возможности попадания в аварию. Чтобы избежать ситуаций, создающих угрозу жизни населения, водитель должен ехать по специально-разработанному маршруту, исключающему места большого скопления людей и производственные объекты.
Другие виды АКБ: можно ли приготовить электролит для них самостоятельно?
Отдельно хотелось бы обратить внимание на современные свинцово-кислотные источники питания — гелевые и AGM. Они также могут быть заправлены собственноручно приготовленным раствором, который в них находится в специфической форме — в виде геля или внутри сепараторов
Для заправки гелевых аккумуляторов понадобится ещё один химический компонент — силикагель, который загустит кислотный раствор.
Кадмиевоникелевые и железоникелевые аккумуляторы
В отличие от свинцовых источников питания, кадмиево- и железоникелевые заливаются щелочным растовром, который является смесью дистиллированной воды и едкого калия или натрия. Гидроксид лития, входящий в состав этого раствора для определённых температурных режимов, позволяет увеличить срок службы АКБ.
Таблица 2. Состав и плотность электролита для кадмиево- и железоникелевых и аккумуляторов.
Железоникелевые источники питания рекомендуется эксплуатировать в тех же условиях, что и кадмиево-никелевые. Однако стоит отметить, что они более восприимчивы к низким температурам. Поэтому их следует использовать до минус 20 градусов.
Состав электролита
Электролит является раствором активного вещества в дистиллированной воде. В зависимости от типа используемых аккумуляторных батарей активным веществом являются:
- серная кислота для свинцово-кислотных аккумуляторов;
- щелочи (едкий натрий или калий) для щелочных аккумуляторов.
В щелочных АКБ для выполнения особых требований в составе электролита может присутствовать добавка едкого лития. Также едкий литий является основным в литий-ионных и литий-полимерных аккумуляторах.
Отличия электролитов для разных типов аккумуляторов
Несмотря на то что принцип работы раствора одинаков для разных источников питания, следует знать о некоторых различиях составов. В зависимости от состава принято выделять щелочной и кислотный электролиты.
Щелочные АКБ
Этот вид источников питания характеризуется наличием гидроокиси никеля, окиси бария и графита. Электролит в этом виде аккумуляторов представляет собой 20% раствор едкого калия. Традиционно используется добавка моногидрата лития, которая позволяет продлить срок эксплуатации АКБ.
Щелочные источники питания отличаются отсутствием взаимодействия калийного раствора с веществами, образуемыми во время работы аккумулятора, что способствует аксимальному уменьшению расхода.
Кислотные АКБ
Этот вид источников питания является одним из самых традиционных, поэтому и раствор в них знаком многим — смесь дистиллированной воды и серного раствора. Концентрат электролита для свинцово-кислотных аккумуляторов дешёво стоит и характеризуется способностью проводить ток большой величины. Плотность жидкости должна соответствовать климатическим показателям.
Таблица 1. Рекомендуемая плотность электролита
Способ развести электролит для щелочного источника питания
Плотность и количество электролита в таких аккумуляторах указана в инструкции по эксплуатации источника питания или на сайте компании-производителя.
Необходимая плотность раствора
Количество твёрдой щелочи равняется количеству электролита, разделенному на
Электролит является важнейшей составляющей аккумуляторных батарей. Без него невозможна их работа и от качества и правильности приготовления зависят как технические параметры, так и долговечность аккумуляторов.
Сейчас в продаже возможно приобретение электролита для любых разновидностей аккумуляторов, но иногда возникает необходимость в его самостоятельном изготовлении. Приготовить электролит для аккумулятора несложно при выполнении ряда условий.
Зачем назначают анализ и как расшифровывают результаты
Следует отметить, что биохимический анализ крови на проверку уровня мочевой кислоты не считается стандартным. Обычно медики назначают его при подозрении на наличие заболеваний, провоцирующих замедление метаболизма или дисфункцию почек.
Забор крови проводят утром натощак, обычно у пациента берут не более 10 мл. Количество метаболита дает медику возможность оценить, в каком состоянии находятся органы и насколько правильно функционируют системы организма.
Если содержание этого вещества в плазме будет повышено, пациенту назначат соответствующее лечение, которое предотвратит скопление избытка солей и урегулирует обмен нуклеиновых кислот.
В некоторых лабораториях бланк с результатами выдают прямо на руки пациенту. Чтобы расшифровать результат самостоятельно, нужно знать, что содержание соединения исчисляется киломолями на литр. Этот показатель обозначает количество молекул, содержащихся в 1 л крови.
О едком и не очень
– Эти идиоты поместили фарфоровый контейнер со «студнем» в специальную камеру, предельно изолированную… То есть это они думали, что камера предельно изолирована, но когда они открыли контейнер манипуляторами, «студень» пошел через металл и пластик, как вода через промокашку, вырвался наружу, и все, с чем он соприкасался, превращалось опять же в «студень». Погибло тридцать пять человек, больше ста изувечено, а все здание лаборатории приведено в полную негодность. Вы там бывали когда-нибудь? Великолепное сооружение! А теперь «студень» стек в подвалы и нижние этажи… Вот вам и прелюдия к контакту.
— А. Стругацкий, Б. Стругацкий «Пикник на обочине»
Привет, %username%!
В том, что я всё ещё что-то пишу — вините вот этого человека. Он навеял идею.
Просто, немного поразмыслив, я решил, что небольшой экскурс по едким веществам получится относительно быстро. Может кому-то будет и интересно. А кому-то — и полезно.
Поехали. Сразу определимся с понятиями.
Едкий — 1. Разъедающий химически. 2. Резкий, вызывающий раздражение, боль. 3. Язвительный, колкий.
Ожегов С.И. Словарь русского языка. — М.: Рус.яз., 1990. — 921 с.
Итак, отбрасываем сразу два последних значения слова. Также отбрасываем «едкие» лакриматоры — которые не столько едкие, сколько вызывают слезотечение, и стерниты — которые вызывают кашель. Да, ниже будут вещества, которые обладают и этими свойствами, но они — что главное! — действительно разъедают материалы, а иногда и плоть.
Мы не будем рассматривать вещества, едкие только для человека и подобных — в виду специфического разрушения мембран клеток. А потому иприты останутся не у дел.
Мы будем рассматривать соединения, которые в комнатных условиях — жидкости. Поэтому жидкий кислород и азот, а также газы типа фтора рассматривать не будем, хотя их можно считать едкими, да.
Как обычно, взгляд будет исключительно субъективным, основанным на собственном опыте. И да — вполне возможно, что кого-то я и не упомню — пиши комментарии, %username%, в течение трёх суток с момента публикации я буду дополнять статью тем, что забылось с самого начала!
И да — у меня нет времени и сил строить «хит-парад», поэтому будет сборная солянка. И со всеми исключениями — она вышла довольно короткой.
Едкие щелочи
А конкретно — гидроксиды щелочных металлов: лития, натрия, калия, рубидия, цезия, франция, гидроксид таллия (I) и гидроксид бария. Но:
- Литий, цезий, рубидий и барий отбрасываем — дорого и редко встретишь
- Если ты, %username%, встретишь гидроксид франция, то едкость тебя будет волновать в последнюю очередь — он жутко радиоактивный
- То же и с таллием — он ядовит до жути.
А потому остались натрий и калий. Но будем откровенны — свойства у всех едких щелочей очень схожие.
Гидроксид натрия известен всем как «каустическая сода» (не путать с пищевой, кальцинированной и другими содами, а также поташем). Гидроксид калия как пищевая добавка Е525 — тоже. По свойствам оба похожи: сильно гигроскопичны, то бишь тянут воду, на воздухе «расплываются». Хорошо растворяются в воде, при этом выделяется большое количество теплоты.
«Расплывание» на воздухе — по сути образование очень концентрированных растворов щелочей. А потому, если положить кусочек едкой щёлочи на бумагу, кожу, некоторые металлы (тот же алюминий) — то по прошествии времени обнаружится, что материал хорошо подъело! То, что показывали в «Бойцовском клубе» — очень похоже на правду: действительно, потные руки — да в щёлочь — будет больно! Лично мне показалось больнее, чем от соляной кислоты (о ней ниже).
Впрочем, если руки очень сухие — скорее всего в именно сухой щёлочи ничего и не почувствуешь.
Едкие щёлочи отлично разваливают жиры на глицерин и соли жирных кислот — так и варят мыло (привет, «Бойцовский клуб!») Чуть дольше, но так же действенно расщепляются белки — то есть в принципе щёлочи плоть растворяют, особенно крепкие растворы — да при нагревании. Недостатком в сравнении с той же хлорной кислотой (о ней тоже ниже) является то, что все щёлочи тянут углекислый газ из атмосферы, а потому сила будет постепенно снижаться. Кроме того, щёлочи реагируют и с компонентами стекла — стекло мутнеет, хотя, чтобы его растворить целиком — тут, конечно, надо постараться.
К едким щелочам иногда относят и тетраалкиламмоний гидроксиды, например
Гидроксид тетраметиламмония
На самом деле в этих веществах объединились свойства катионных поверхностно-активных веществ (ну это как обычное мыло — только катионное: тут активная дифильная частица — с зарядом «+», а в мыле — с зарядом «-«) и относительно высокая основность. Если попадёт на руки — можно намылить в воде и помыть, как мылом, если в водном растворе погреть волосы, кожу или ногти — растворятся. «Едкость» на фоне гидроксидов натрия и калия — так себе.
Серная кислота
H2SO4
Самая популярная, наверное, во всех историях. Не самая едкая, но достаточно неприятная: концентрированная серная кислота (которая 98%) — маслянистая жидкость, которая очень любит воду, а потому у всех её отнимает. Отнимая воду у целлюлозы и сахара, обугливает их. Точно так же она радостно отнимет воду и у тебя, %username%, особенно если налить её на нежную кожу лица или в глаза (ну в глаза на самом деле всё будет попадать с приключениями). Особо добрые люди мешают серную кислоту с маслом, чтобы труднее смывалась и лучше впитывалась в кожу.
Кстати, забирая воду, серная кислота здорово разогревается, что делает картину ещё больше сочной. А потому смывать её водой — очень плохая идея. Лучше — маслом (смывать, а не втирать — а потом уже смыть водой). Ну или большим потоком воды, чтобы сразу и охлаждать.
«Сначала вода, а потом кислота — иначе случится большая беда!» — это именно про серную кислоту, хотя почему-то все считают, что про любую кислоту.
Будучи окислителем, серная кислота окисляет поверхность металлов до оксидов. А поскольку взаимодействие оксидов с кислотами проходит при участии воды как катализатора — а воду серная кислота не отдаёт — то происходит эффект, называемый пассивацией: плотная, нерастворимая и непроницаемая плёнка оксида металла защищает его от дальнейшего растворения.
По этому механизму концентрированную серную кислоту посылают в далёкие дали железо, алюминий. Примечательно, что если кислоту разбавить — появляется вода, и посылать не получается — металлы растворяются.
Кстати, оксид серы SO3 растворяется в серной кислоте и получается олеум — который иногда ошибочно пишут как H2S2O7, но это не совсем верно. У олеума тяга к воде ещё больше.
Собственные ощущения от попадания серной кислоты на руку: немного тепло, потом чуток печёт — смыл под краном, ничего страшного. Фильмам не верьте, но на лицо капать не советую.
Органики часто пользуются хромпиком или «хромовой смесью» — это бихромат калия, растворённый в серной кислоте. По сути это — раствор хромовой кислоты, он хорош для мытья посуды от остатков органики. При попадании на руку тоже жжётся, но по сути — серная кислота плюс токсичный шестивалентный хром. Дырок в руке не дождёшься, разве что на одежде.
Автор этих строк знаком с идиотом, который вместо бихромата калия использовал перманганат калия. При контакте с органикой немножко жахнуло. Присутствующие обделались отделались лёгким испугом.
Кстати, раз уж вспомнили хромпик — немного отвлечёмся от темы кислот и
Хлористый хромил
CrO2Cl2
По сути своей — лютое соединение шестивалентного хрома и соляной кислоты. Тёмно-красная жидкость, которая тянет воду, гидролизуется — и в итоге дымит этой самой соляной кислотой. Едкость — итог этого братского единения: хром — окисляет, соляная кислота — растворяет: воспламеняет некоторые органические растворители (спирт, скипидар), однако в некоторых растворяется (четыреххлористый углерод, дихлорметан, сероуглегод). Подъедает металлы, но не настолько хорошо, как кислоты — опять дело в пассивации. например, сталь при воздействии приобретает красивую тёмно-синию поверхность.
Кожу — понятно — изъязвляет, при чём в этом сильнее хромпика, поскольку лучше проникает в кожу как в неполярную органическую ткань. Но дело даже не в этом, а в шестивалентном хроме, который вообще-то канцероген, а потому глубже проникнет — больше проблем. Ну и конечно надышаться куда опаснее.
Соляная кислота
HCl
Выше 38% в воде не бывает. Одна из самых популярных кислот для растворения — в этом она покруче остальных, потому что технологически может быть очень чистой, а кроме действия, как кислота, ещё и образует комплексные хлориды, которые повышают растворимость. Кстати, именно по этой причине нерастворимый хлорид серебра очень даже растворим в концентрированной соляной кислоте.
Эта при попадании на кожу жжётся чуток сильнее, субъективно — ещё и зудит, к тому же воняет: если в лаборатории с плохой вытяжкой работать много с концентрированной соляной кислотой — твой стоматолог скажет тебе «спасибо»: ты его озолотишь на пломбах. Кстати, помогает жвачка. Но не сильно. Лучше — вытяжка.
Поскольку не маслянистая и с водой сильно не разогревается, то едкость — только к металлам, и то не ко всем. Кстати, сталь в концентрированной соляной кислоте пассивируется и говорит ей «не-а!». Чем и пользуются при транспортировке.
Азотная кислота
HNO3
Тоже очень популярная, её тоже почему-то боятся — а зря. Концентрированная — это которая до 70% — она самая популярная, выше — это «дымящая», чаще всего никому не нужная. Есть ещё безводная — так та ещё и взрывается.
Будучи окислителем, пассивирует многие металлы, которые покрываются нерастворимой плёнкой и говорят: «до свидания» — это хром, железо, алюминий, кобальт, никель и другие.
С кожей моментально реагирует по принципу ксантопротеиновой реакции — будет жёлтое пятно, что означает, что ты, %username%, всё-таки состоишь из белка! Через какое-то время жёлтая кожа слезет, как при ожоге. При этом щиплет меньше соляной, хотя воняет не хуже — и на этот раз токсичнее: летящие окислы азота не очень хороши для организма.
В химии используют так называемую «нитрующую смесь» — самая популярная состоит из серной и азотной кислот. Используется в синтезах, в частности в получении весёлого вещества — пироксилина. По едкости — тот же хромпик плюс красивая жёлтая кожа.
Так же есть «царская водка» — это часть азотной кислоты на три части соляной. Используется для растворения некоторых металлов, в основном — драгоценных. На разном соотношении и добавлении воды основан капельный метод проверки пробы золотых изделий — кстати, специалистов по этому методу очень сложно надурить с подделкой. По едкости для кожи — та же «нитрующая смесь» плюс воняет отменно, запах не спутаешь ни с чем, он тоже довольно токсичный.
Есть ещё «обратная царская водка» — когда соотношение наоборот, но это редкая специфика.
Кстати, о той самой «дымящей», которая красная, злая и окислитель — цитирую рассказ хорошего друга, который мне вот прямо сейчас прислал.
Гнал я эту самую 98% азотку. То ли просто перегонял для очистки, то ли из меланжа, уже не помню. Нагнал литра два, снимаю приемник. Прошу лаборантку дать чистую колбу на 2 литра — перелить. Она мне и дала сухую, чистую, но из под спирта — и с закрытой пробкой. То есть пары были и накопились. Я туда воронку и переливаю. Я ее туда — а она обратно. Хорошо брызнула на руки, на рожу и ниже шеи. Ощущение — как орел в морду вцепился. Плюс руки, шея, под носом ну и т.д. по мелочи. В руках, напоминаю, два литра того же добра. Глаза закрыты, естественно. Понимаю, что бросить колбу нельзя, будет сразу сильно хуже. Аккуратно ставлю колбу на резиновую подставку, перемещаюсь к мойке, разворачиваю гусак себе в морду и включаю полный напор. Секунд за пять управился. До подкожной клетчатки не добралась. А то все было бы намного хуже. Видел у другого мужика, что бывает через 10-15 сек. Труднозаживающие багровые рубцы на половину руки. Потом понял, почему она такая злая. Мало того, что довольно сильная кислота и окислитель, она еще и чудесный растворитель. Неограниченно смешивается с водой, но неограниченно смешивается и с, например, дихлорэтаном. Такая себе бифильная дрянь.
Фосфорная кислота
H3PO4
На самом деле я привёл формулу ортофосфорной кислоты — самой распространённой. А есть ещё метафосфорная, полифосфорные, ультрафосфорные — короче, хватает, но неважно.
Концентрированная ортофосфорная кислота (85%) — это такой сиропчик. Кислота она сама по себе средняя, её часто используют в пищевой промышленности, кстати — когда тебе ставят пломбы, то поверхность зуба предварительно протравливают фосфорной кислотой.
Коррозионность у неё так себе, но есть неприятный нюанс: этот сиропчик хорошо впитывается. Поэтому если капнет на вещи — впитается, а потом будет потихоньку разъедать. И если от азотной и соляной кислоты будет пятно или дырка — то от фосфорной вещь будет разлазиться, особенно это красочно на обуви, когда дырка как бы крошится, пока не получится насквозь.
Ну а вообще едкой её назвать сложно.
Плавиковая кислота
HF
Концентрированная плавиковая кислота — это примерно 38%, хотя и бывают странные исключения.
Слабенькая кислота, которая берёт яростной любовью фторид-ионов образовывать стойкие комплексы со всем, с кем можно. Поэтому на удивление растворяет то, что другие, более сильные подруги — не могут, а потому очень часто используется в разных смесях для растворения. При попадании на руку ощущения будут больше от других компонентов таких смесей, но есть нюанс.
Плавиковая кислота растворяет SiO2. То есть песок. То есть стекло. То есть кварц. Ну и так далее. Нет, если ты плеснёшь на окно этой кислотой — оно не растворится, но мутное пятно останется. Чтобы растворить — нужно долго держать, а ещё лучше — нагреть. При растворении выделяется SiF4, который так полезен для здоровья, что лучше это делать под вытяжкой.
Маленький, но приятный нюанс: кремний содержится у тебя, %username%, в ногтях. Так вот, если плавиковая кислота попадёт под ногти — ты ничего не заметишь. Но ночью спать не сможешь — болеть будет ТАК, что иногда возникает желание оторвать палец. Поверь, друг — я знаю.
И вообще плавиковая кислота токсична, канцерогенна, впитывается через кожу и масса всего — но мы-то сегодня про едкость, правда?
Помнишь, мы договаривались в самом начале, что фтора не будет? Его и не будет. Но будут…
Фториды инертных газов
На самом деле фтор — суровый парень, с ним особо не повыпендриваешься, а потому некоторые инертные газы образуют с ним фториды. Известны такие стабильные фториды: KrF2, XeF2, XeF4, XeF6. Всё это — кристаллы, которые на воздухе с разной скоростью и охотой разлагаются влагой до плавиковой кислоты. Едкость — соответствующая.
Иодоводородная кислота
HI
Самая сильная (по степени диссоциации в воде) бинарная кислота. Сильный восстановитель, чем пользуются химики-органики. На воздухе окисляется и становится бурой, чем и пачкает при контакте. Ощущения при контакте — как от соляной. Всё.
Хлорная кислота
HClO4
Одна из самых сильных (по степени диссоциации в воде) кислот вообще (с ней конкурируют суперкислоты — о них ниже) — функция кислотности Гаммета (численное выражение способности среды быть донором протонов по отношению к произвольному основанию, чем меньше — тем сильнее кислота) составляет -13. Безводная — сильный окислитель, любит взрываться, да и вообще неустойчива. Концентрированная (70%-72%) — окислитель не хуже, часто используют в разложении биологических объектов. Разложение интересно и захватывающе тем, что может взрываться в процессе: нужно следить, чтобы не было частиц угля, чтобы не кипело слишком бурно и т.д. Хлорная кислота к тому же довольно грязная — её невозможно очистить субперегонкой, взрывается зараза! Поэтому используют её нечасто.
При попадании на кожу жжётся, ощущения как от соляной. Воняет. Когда видите в фильмах, что кто-то кинул труп в ёмкость с хлорной кислотой — и он растворился, то да, такое возможно — но долго или греть. Если греть — может рвануть (см. выше). Так что будьте критичны к кинематографу (я, кажется, видел это в «Кловерфилд, 10»).
Кстати, едкость оксида хлора (VII) Cl2O7 и оксида хлора (VI) Cl2O6 — это итог того, что с водой эти оксиды образуют хлорную кислоту.
А теперь представим, что мы решили в одном соединении объединить сильную кислотность — и едкость фтора: возьмём молекулу хлорной или серной кислоты — и заменим на ней все гидроксильные группы на фтор! Дрянь получится редкостная: она будет взаимодействовать с водой и подобными соединениями — и будет в месте реакции сразу получаться сильная кислота и плавиковая кислота. А?
Фториды серы, брома и иода
Помните, мы договорились рассматривать только жидкости? По этой причине в нашу статью не попал трифторид хлора ClF3
, который кипит при +12 °C, хотя все страшилки о том, что он жутко токсичен, воспламеняет стекло, противогаз и при разливании 900 килограммов — проедает 30 см бетона и метр гравия — всё это правда. Но мы же договорились — жидкости.
Однако есть жёлтая жидкость — пентафторид иода IF5
, бесцветная жидкость —
трифторид брома BrF3
, светло-жёлтая —
пентафторид брома BrF5
, которые не хуже. BrF5, к примеру, тоже растворяет стекло, металлы и бетон.
Аналогично — среди всех фторидов серы жидким является только декафторид дисеры (иногда её называют ещё пятифтористой серой) — бесцветная жидкость с формулой S2F10
. Но это соединение при обычных температурах достаточно стабильно, не разлагается водой — а потому не особо и едко. Правда, в 4 раза токсичнее фосгена с аналогичным механизмом действия.
Кстати, говорят, что пентафторид иода был «специальным газом» для заполнения атмосферы в спасательном шаттле в последних кадрах фильма «Чужой» 1979 года. Ну не помню, честно. Напомнился! Блин, там настолько круто, что я не удержался — и посвятил этому отдельную статью.
Даже нашёл, присмотрелся и понял, что Рипли там жила в таких суровых условиях, что инопланетный зверь — просто няшка
Суперкислоты
Термин «суперкислота» введён Джеймсом Конантом в 1927 году для классификации более сильных кислот, чем обычные минеральные кислоты. В некоторых источниках хлорную кислоту относят к суперкислоте, хотя это не так — она обычная минеральная.
Ряд суперкислот — это минеральные, к которым подцепили галоген: галоген тянет на себя электроны, все атомы очень сильно гневаются, а достаётся всё как обычно водороду: тот отваливается в виде Н+ — бабах: вот и кислота стала сильнее.
Примеры — фторсерная и хлорсерная кислоты
У фторсерной кислоты функция Гаммета -15,1, кстати, благодаря фтору, эта кислота постепенно растворяет пробирку, в которой хранится.
Потом кто-то из умных подумал: а давайте возьмём кислоту Льюиса (вещество, способное принять пару электронов другого вещества) и смешаем с кислотой Бренстеда (веществом, которое способно отдавать протон)! Смешали пентафторид сурьмы с плавиковой кислотой — получили гексафторсурьмяную кислоту HSbF6
. В этой системе плавиковая кислота выделяет протон (H+), а сопряжённое основание (F−) изолируется координационной связью с пентафторидом сурьмы. Так образуется большой октаэдрический анион (SbF6−), являющийся очень слабым нуклеофилом и очень слабым основанием. Став «свободным», протон обусловливает сверхкислотность системы — функция Гаммета -28!
А потом пришли другие и сказали, а чего это кислоту Бернстеда взяли слабую — и придумали вот что.
Трифторметансульфоновая кислота
— сама по себе уже суперкислота (функция Гаммета -14,1). Так вот, к ней добавили опять пентафторид сурьмы — получили снижение до -16,8! Такой же фокус с фторсерной кислотой дал снижение до -23.
А потом группа ученых с химической кафедры американского университета Калифорнии под управлением профессора Кристофера Рида затусила с коллегами из Института катализа СО РАН (Новосибирск) и придумали карборановую кислоту H(CHB11Cl11). Ну «карборановой» её назвали для обычных людей, а если хочешь почувствовать себя учёным — произнеси «2,3,4,5,6,7,8,9,10,11,12-ундекахлор-1-карба-клозо-додекаборан(12)» три раза и быстро.
Так выглядит эта красотка
Это — сухой порошочек, который растворим в воде. Это и есть Самая Сильная Кислота на текущий момент. Карборановая кислота приблизительно в миллион раз сильнее концентрированной серной кислоты. В обычных шкалах измерить силу кислоты не удается, так как кислота протонирует все известные слабые основания и все растворители, в которых она растворяется, включая воду, бензол, фуллерен-60, диоксид серы.
Впоследствии Кристофер Рид в интервью службе новостей Nature сказал: «Идея синтеза карборановой кислоты родилась из фантазий «о молекулах, никогда прежде не создаваемых». Вместе с коллегами он хочет использовать карборановую кислоту для окисления атомов инертного газа ксенона — просто потому, что никто прежде этого не делал. Оригинально, что сказать.
Ну поскольку суперкислоты — это обычные кислоты, то и действуют они обычно, только немного сильнее. Ясно, что кожу будут жечь, но это не значит — что растворять. Фторсульфоновая — отдельный случай, но там всё благодаря фтору, как и в плавиковой.
Тригалогенуксусные кислоты
А конкретно — трифторуксусная и трихлоруксусная кислота
Милы и приятны сочетанием свойств органического полярного растворителя и достаточно сильной кислоты. Воняют — похоже на уксус.
Самая няшка — трифторуксусная кислота: 20%-ный раствор разрушает металлы, пробку, резину, бакелит, полиэтилен. На коже жжётся и образует сухие язвы, доходящие до мышечного слоя.
Трихлоруксусная в этом плане — младший брат, но тоже ничего. Кстати, аплодисменты слабому полу: в погоне за красотой, некоторые идут на так называемую процедуру ТСА-пилинга (ТСА — это TetraChloroAcetate) — когда этой самой трихлоруксусной кислотой растворяют верхний огрубевший слой кожи.
Правда, если косметолог заболтается по телефону, возможен фэйл
Уксусная кислота
СН3СООН
Скорее всего, у тебя на кухне есть эта кислота — и да, она используется как пищевая добавка Е260. Но также она бывает и покрепче — 70-80%-й водный раствор уксусной кислоты называют уксусной эссенцией, а если концентрация близка к 100% — ледяной уксусной кислотой (потому что она может замерзать и образовывать нечто похожее на лёд.
Уксусная кислота не так едка по отношению к металлам, как минеральные кислоты, но поскольку и не так полярна, а в какой-то степени даже дифильна (сочетание гидрофобной и гидрофильной части в одной молекуле — как в поверхностно-активных веществах) — то она здорово всасывается кожей. Опасными считаются растворы с концентрацией уксусной кислоты больше 30%. Особенность ожогов в том, что также инициируется развитие коагуляционных некрозов прилегающих тканей различной протяженности и глубины — если не смыть, то будут долго заживающие язвы и рубцы.
Ну и воняет она, конечно, знатно.
Муравьиная кислота
НСООН
Мы уже обсуждали, что муравьиная кислота, образующаяся в организме после принятия метанола, — одна из основных причин его токсичности. Так вот, муравьиная кислота извне вовсе не так опасна, поскольку быстро метаболизируется и выводится организмом. Токсичность довольно низка — для крыс LD50 порядка 1,8 г/кг, а потому муравьиную кислоту тоже часто используют, в том числе и как пищевую добавку — и этого бояться не стоит.
»Едкость» муравьиной кислоты зависит от концентрации. Согласно классификации Европейского союза, концентрация до 10% обладает раздражающим эффектом, больше 10% — разъедающим. И речь опять не о металлах и стекле — а об организме. При контакте с кожей 100%-я жидкая муравьиная кислота вызывает сильные химические ожоги. Попадание даже небольшого её количества на кожу причиняет сильную боль, поражённый участок сначала белеет, как бы покрываясь инеем, потом становится похожим на воск, вокруг него появляется красная кайма. Кислота легко проникает через жировой слой кожи, поэтому промывание поражённого участка раствором соды необходимо произвести немедленно. Так что муравьи действительно что-то знают.
Бром
Br2
Тяжёлая едкая жидкость красно-бурого цвета с сильным неприятным запахом, отдалённо напоминающим запах одновременно иода и хлора. Кстати, название «бром» от греческого βρῶμος — «вонючка», «вонючий».
Бром — типичный галоген, по химической активности бром занимает промежуточное положение между хлором и иодом. То есть не такой прыткий, как фтор — но поживее скучного иода. И да, до хлора тоже не дотягивает.
Немного растворим в воде, хорошо — в некоторых органических растворителях. Бромная вода — реактив на непредельные углеводороды — воняет, но вполне себе мирная и ничего сильно не растворяет.
Чистый бром могуч, вонюч и волосат, а также токсичен. При попадании на кожу вызывает ожоги: неприятность в том, что молекулы брома неполярны, а потому хорошо проникают в гидрофобную человеческую кожу и плоть — а потому ожоги действительно болезненны, долго заживают, почти всегда оставляют на память шрам. Алюминий вспыхивает при контакте с бромом, остальные металлы более воздержаны, но в виде порошка — некоторые реагируют, например, железо.
Бетон и стекло к брому достаточно устойчивы. Органические соединения бромом — что? — правильно! — бромируются при наличии ненасыщенной связи. По этой причине устойчивость полимеров зависит от их типа, к примеру полиэтилен и полипропилен — плевать хотели на бром при комнатных условиях.
Пероксид водорода
H2O2
Нестабильное соединение, которое постоянно постепенно разваливается на кислород и воду. Чем выше концентрация — тем нестабильнее, что постепенно превращается во взрывоопасность. Для стабилизации технического пероксида водорода в него добавляют пирофосфат или станнат натрия; при хранении в алюминиевых емкостях используют ингибитор коррозии — нитрат аммония.
Пероксид водорода в лаборатории обычно представляет собой раствор 38%. При попадании на кожу оказывает химический ожог с характерным белым окрашиванием. Ожог болезненный, особенно на тонкой коже, побелевшая ороговевшая кожа потом часто трескается и зудит.
В медицине используют 3% пероксид водорода для очистки глубоких ран сложного профиля, гнойных затёков, флегмон и других гнойных ран, санация которых затруднена — так вещество обладает не только антисептическим эффектом, но и создаёт большое количество пены при взаимодействии с ферментом каталазой. Это в свою очередь позволяет размягчить и отделить от тканей некротизированные участки, сгустки крови, гноя, которые будут легко смыты последующим введением в полость раны антисептического раствора. Кстати, перекись водорода нежелательна в других случаях ран: обладая хорошими очищающими свойствами, это вещество на самом деле не ускоряет процесс заживления, поскольку повреждает прилегающие к ране клетки, равно как и молодые, новообразующиеся ткани — а это ещё и чревато образованием рубцов.
Кроме как ожогов на коже — ничего не разъедает и не растворяет. Металлы, стекло и пластики устойчивы к пероксиду водорода.
А ещё пероксид водорода подарил миру много уникальных натуральных блондинок с чёрными корнями волос!
Близки к пероксиду водорода так называемые надкислоты — кислоты, в которых присутствуют пероксидные группы. Пример: надуксусная кислота СН3СОООН
— вещество, напоминающее по свойствам пероксид водорода, а потому и использующееся точно в таких же сферах. Есть «первомур» или «С-4» (нет, это не тот С-4, о котором ты подумал) — это
пермуравьиная кислота HCOOOН
, которая ещё слабее надуксусной, а потому хирируги моют ей руки перед операцией. И наконец —
трифторперуксусная кислота СF3СОООН
— лютый, бешеный окислитель, на который с восхищением смотрят химики-органики за возможность окисления анилина до нитробензола, получения гипервалентного иода в органических соединениях, реакцию Байера-Виллигера и другие малопонятные нормальным людям вещи. По едкости — трифторуксусная кислота, смешанная с перекисью водорода, чем, собственно, и является, а потому для рук представляет особую опасность, да. В виду своей высокой окислительной способности, трифторперуксусная кислота не продаётся, а обычно получается восхищающимися химиками-органиками прямо там, где необходимо, взаимодействием трифторуксусного ангидрида с пероксидом водорода.
Ну вот примерно так, если говорить про жидкость и про едкость. Будут ещё дополнения?